Produktion von trägerfreiem 177Lu am FRM II für radiopharmazeutische Anwendungen
Radiochemie München RCM in Zusammenarbeit mit Isotope Technologies Garching GmbH (ITG)
Wissenschaftler: Dr. Christoph Barkhausen, Dr. Konstantin Zhernosekov
Gefördert von der Bayerischen Forschungsstiftung (BFS)
Durch erfolgreiche klinische Ansätze in der Endoradiotherapie und Brachytherapie wächst die Nachfrage nach dem Reaktornuklid 177Lu weltweit. Sehr hohe Anforderungen an die Qualität des Nuklids erschweren allerdings den Herstellungsprozess und dadurch die Zugänglichkeit.
Zielsetzung dieses Projektes war somit die Entwicklung einer chemischen Verfahrensweise, um 177Lu trägerfrei (non carrier added [n.c.a.] 177Lu) an der Hochfluss-Neutronenquelle FRM II in Garching herzustellen und die erste europaweite Produktion nach den Anforderungen des Arzneimittelgesetzes zu etablieren. Zu diesem Zweck wurden präparativ-chromatographische Methoden entwickelt und eingesetzt. Im Anschluss daran wurde in abgeschirmten Heißen Zellen eine Routineproduktion von n.c.a.177Lu in industriellen Mengen etabliert.
Der niederenergetischen β-Strahler 177Lu (T½ = 6.71 d) bildet ein perfektes Vehikel zur gezielten Deponierung großer Energiemengen in kleinen Volumina. Diese physikalischen Eigenschaften werden in Form der Radioimmuno- und Peptidrezeptor-Radionuklid-Therapie mit vielversprechenden Ergebnissen vorwiegend zur Behandlung maligner Erkrankungen eingesetzt. Eine erfolgreiche Anwendung des Reaktornuklids 177Lu ist allerdings durch die produktionstechnisch erzielbare spezifische Aktivität des Nuklids [Bq/mg] und die Reinheit bestimmt. Eine hohe spezifische Aktivität des Radionuklids ist notwendig, um eine möglichst hohe spezifische Aktivität und damit optimale, eingesetzte Mengen des Radiotherapeutikums zu erreichen. Wird keine hohe spezifische Aktivität und Reinheit erreicht, so kann dies unter anderem zu einer negativen Beeinflussung der Herstellung des Radiotherapeutikums führen.
177Lu kann durch folgende Kernreaktionen erzeugt werden:
(1) 176Lu(n,γ)177Lu;
(2) 176Yb(n,γ)177Yb →177Lu
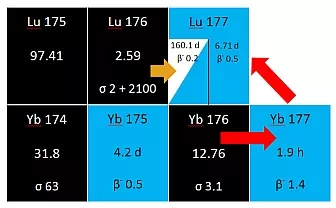
Abbildung 1: Ausschnitt aus der Nuklidkarte; Reaktionswege zur Herstellung von 177Lu: gelber Pfeil stellt den direkten Reaktionspfad, die roten Pfeile stellen den indirekten dar
Die Kernreaktion (1) stellt die Neutroneneinfangreaktion an 176Lu dar, welche in letzter Konsequenz zu geträgertem 177Lu und dadurch zu limitierter Produktqualität führt. Durch die Bestrahlung von 176Lu wird zusätzlich das in medizinischer und strahlenschutztechnischer Hinsicht unerwünschte, langlebige Radionuklid 177mLu (T½ = 160.1 d) erzeugt (Abbildung 1). Der Anteil des 177mLu kann je nach Bestrahlungsparameter bis zu 0.1 % der 177Lu-Aktivität betragen. Im Hinblick auf die Anwendung am Menschen und angesichts der hohen zu produzierenden Gesamtaktivitäten ist diese Verunreinigung kritisch zu sehen. Im Rahmen der Behandlungen besteht ein anhaltendes erhöhtes Risiko der 177mLu-Freisetzung in die Umwelt, bedingt durch die lange Halbwertszeit des Nuklids. Darüber hinaus steht der Verbraucher in der Klinik vor dem Problem der sicheren Handhabung und Entsorgung der Restmengen eines langlebigen Nuklids, welches durch die in Kliniken übliche Lagerung der radioaktiven Abfälle kaum zu lösen ist.
Die attraktivere und medizinisch und kommerziell sinnvollere aber technisch anspruchvollere Option, ist die Herstellung von trägerfreiem 177Lu über die indirekte Kernreaktion (2). Durch die Bestrahlung von hoch angereicherten (> 99 %) 176Yb wird das kurzlebige Radioisotop 177Yb (T½ = 1.9 h) erzeugt, welches zu 177Lu zerfällt (Abbildung 1). In diesem Fall ist das Zielnuklid 177Lu ein Isoton zum Targetnuklid 176Yb und kann daher chemisch in trägerfreier Form isoliert werden. Da durch den Zerfall des Nuklids 177Yb kein 177mLu entsteht, wird das 177Lu mit einer sehr hohen Radionuklidreinheit hergestellt.
Der Nachteil bei der Wahl dieser Strategie ist das notwendige radiochemische Verfahren zur Trennung des Yb(makro)/177Lu(mikro)-Systems. Da das Ziel- und das Targetnuklid zwei benachbarte Elemente in der Lanthanidenreihe sind, bleibt die Abtrennung auf Grund ihrer chemischen Ähnlichkeit eine große Herausforderung. Außerdem wird die Aufgabe durch den Einsatz von massiven 176Yb Targets noch komplexer.
Der auf Basis der Kationenaustauschchromatographie entwickelte Prozess ermöglicht die Aufbereitung von Targetmassen bis zu 150 mg mit Ausbeuten an n.c.a.177Lu bis zu 95 %. Das an der Radiochemie München evaluierte System wurde bei ITG erfolgreich in einer Heißen Zelle in Form eines semi-automatischen Prozesses installiert. Die Routineproduktion von n.c.a.177Lu in industriellen Mengen wurde etabliert und beinhaltet das Handling des hochaktiven Targets, die chemische Isolierung von 177Lu und den Transfer des Produktes in die entsprechende, chemische Form. Um die pharmazeutische Qualität des Produktes und die Herstellungserlaubnis zu erlangen, wurde das System in eine Reinraumumgebung überführt.